基因剪輯在抗疫實驗立功 有機會發展出新療法 – 中央社發布於2021年7月13日
先來認識什麼是 CRISPR(Clustered Regularly Interspaced Short Palindromic Repeats),唸起來像是形容詞「易脆的(Crisp)」之比較級Crisper
由於 CRISPR-Cas9 是從細菌基因組系統發展而來的,因此它可用於靶向病毒中的遺傳物質。具體而言,藉由兩個RNA分子(crRNA 和 tracrRNA)特異性識別位點,共同引導Cas9蛋白酶靶向病毒基因組的特定部位,藉此阻止雙股DNA病毒執行其正常功能。影片提及的杜德納與夏彭蒂耶,由於對 CRISPR-Cas9 基因編輯技術的貢獻而共同獲得2020年諾貝爾化學獎。
Cas是CRISPR相關蛋白(CRISPR-associated proteins, Cas)的簡稱,CRISPR/Cas9系統是目前研究最深入、技術最成熟的一種類別。雖然Cas9是第一個被廣泛應用的CRISPR核酸酶(由1368個胺基酸組成),然而此系統仍有它的不足之處,就是影片中提及的脫靶效應。
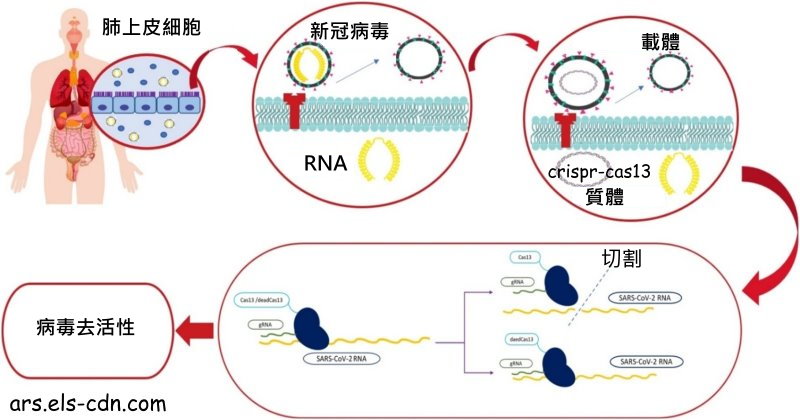
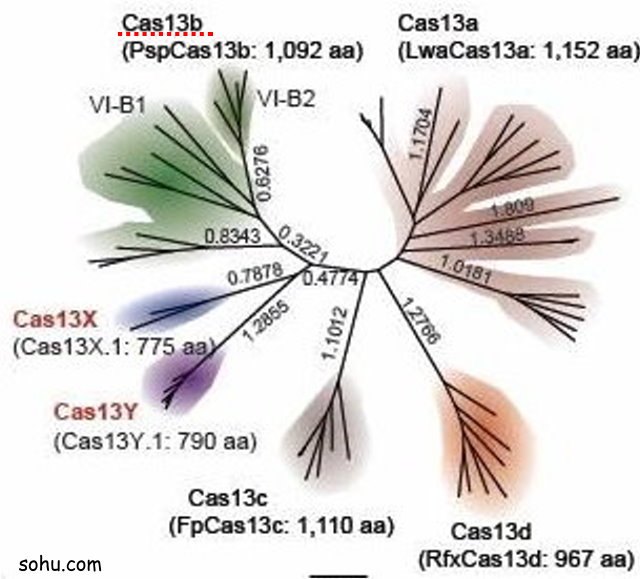
至於新聞中提及的 Cas13b 則是一種只靶向單股RNA 的CRISPR核酸酶(由1092個胺基酸組成),不同於Cas9須藉助crRNA和tracrRNA來實現對目標DNA的識別和切割,Cas13只需要一個crRNA(CRISPR RNA)即可實現對目標RNA的切割。在 crRNA 引導下特異切割單鏈靶 RNA,並有非特異性的附帶切割(collateral effect)能力,這種特性已被應用於開發各種診斷的技術
2015年,美國Eugene Koonin實驗室和來自MIT的張峰團隊合作,利用 計算生物學 方法在微生物巨集基因組資料庫中發現了Cas13a、Cas13b和Cas13c三種系統,並證明了這些系統在哺乳動物細胞中可以對靶標RNA進行有效的降低特定基因功能之表達(gene knock-down)。2017年的這篇研究論文”RNA targeting with CRISPR–Cas13“,張峰研究團隊證實該系統在人體細胞和在細菌中不同的地方是Cas13a僅靶向crRNA指定的RNA,而讓細胞中測序的所有其他的RNA保持完整,這對於降解crRNA靶向的入侵性RNA,具有廣泛的潛在應用價值
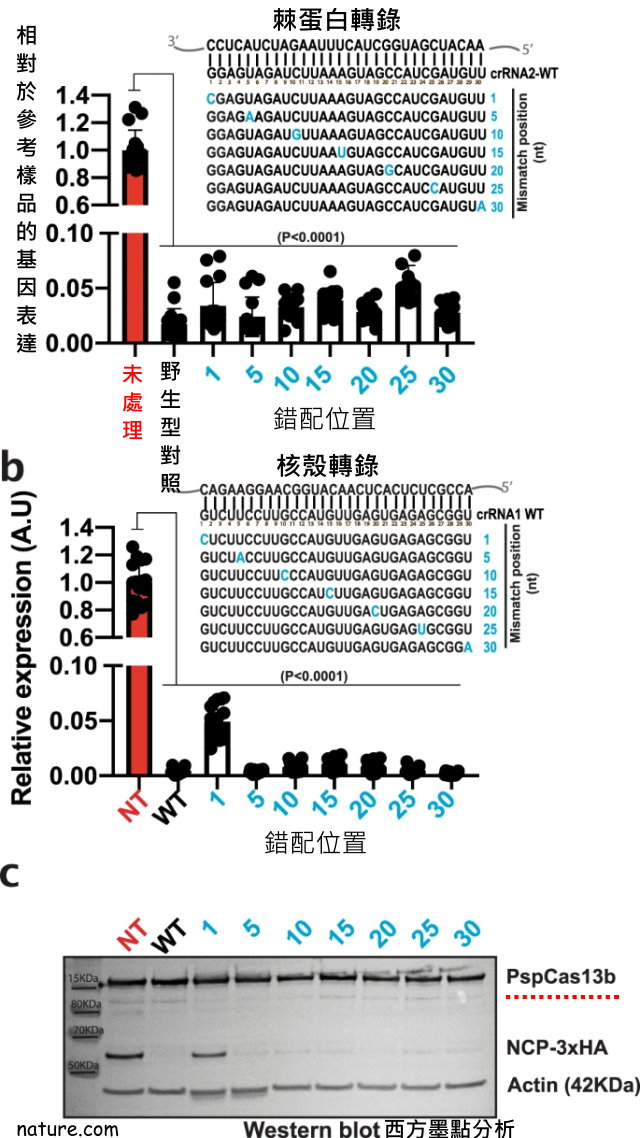
病毒變異主要是透過容易出錯的聚合酶引起的單核苷酸插入/缺失所造成,來自澳洲的莎朗·李文團隊則研究了 PspCas13b 的crRNA與其靶標之間錯配的耐受性。研究團隊設計了靶向 Spike (crRNA2) 或核殼 (crRNA1) 轉錄本的 crRNA,使其在間隔位置 1、5、10、15、20、25 和 30 處具有單核苷酸錯配,並將它們的基因沈默效率比對完全匹配的野生型對應物
研究結果表明這項沈默技術對不同位置的單核苷酸錯配具有良好的耐受性,其對靶標沈默沒有明顯影響。這項數據突顯出 PspCas13b 能夠對新冠病毒的自發突變保持有效,具有克服突變驅動的病毒逃逸之潛力。