2016/11/6 еҢ—жө·йҒ“еӨ§йӣӘеүө21е№ҙдҫҶзҙҖйҢ„пјҢжҘөең°жёҰж—ӢеҶҚеәҰй—ңдёҚдҪҸеҢ—жҘөеҜ’йўЁпјҢйҡЁеҫҢжқұдә¬еёӮдёӯеҝғеңЁ11/25йҷҚдёӢ54е№ҙдҫҶйҰ–ж¬Ўзҡ„11жңҲеҲқйӣӘ
д»ҠеӨ©дҫҶиҒҠиҒҠеңЁйҒ“и·ҜдёҠж’’й№ҪиғҪиһҚеҶ°зҡ„ж©ҹеҲ¶
гҖҢQпјҡеҶ°йӣӘдёҠж’’й№ҪпјҢзӮәдҪ•еҸҜе°Үе…¶иһҚеҢ–пјҹгҖҚ
гҖҢAпјҡйҖҷжҳҜеӣ зӮәж’’й№ҪеҸҜд»ҘпЁүдҪҺеҶ°йӣӘзҡ„зҶ”й»һгҖҚ
йҖҷеҸҘи©ұдјјд№ҺжҳҜзңҫжүҖзҡҶзҹҘзҡ„еёёп§јпјҢиҖҢйҖҷзЁ®и§Җй»һд№ҹпҘӢпЁҠж–јеҗ„科жҷ®ж–Үз« дёӯпјҢдёҚйҒҺйҖҷзЁ®иӘӘжі•жңүиӘӨгҖӮзңҹжӯЈзҡ„еҺҹеӣ е…¶еҜҰе°ұйҡұи—ҸеңЁеӨ§е®¶е°ҸеӯёжҷӮжӣҫеҒҡйҒҺзҡ„дёҖеҖӢеҶ·еҠ‘еҜҰй©—дёӯпјҢеҲ©з”ЁеңЁеҶ°еЎҠдёӯеҠ е…ҘйЈҹй№ҪдҫҶйҷҚдҪҺжә«еәҰ
зҶ”й»һжҳҜзҙ”зү©иіӘзҡ„зү©зҗҶзү№жҖ§пјҢиғҪеӨ ж”№и®Ҡе®ғзҡ„еҸӘжңүеЈ“еҠӣ
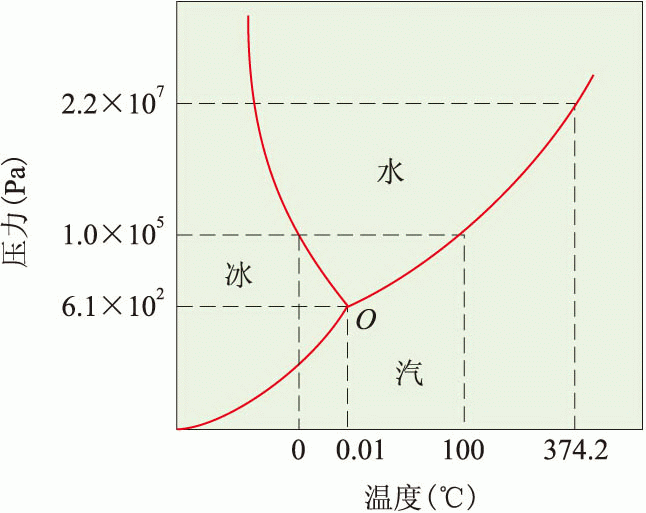
з”ұж°ҙзҡ„дёүзӣёең–дёӯеҸҜзҹҘпјҢиӢҘеўһеӨ§еЈ“еҠӣеүҮж°ҙзҡ„жІёй»һжңғдёҠеҚҮпјҲex.еЈ“еҠӣйҚӢпјүпјҢеҮқеӣәй»һеүҮжңғдёӢйҷҚпјҲex.еҫ©еҶ°зҸҫиұЎпјү
з”ұж–јеңЁеҶ°йӣӘдёҠж’’й№Ҫд»ҘеҫҢе°ұеҪўжҲҗдәҶж··еҗҲзү©пјҢ既然已經дёҚжҳҜзҙ”зү©иіӘдәҶпјҢжҖҺйәјйӮ„иғҪиӘӘжҳҜж”№и®ҠдәҶйӣӘзҡ„зҶ”й»һе‘ўпјҹе…¶еҜҰж”№и®Ҡзҡ„жҳҜй№Ҫж°ҙзҡ„еҮқеӣәй»һпјҢжҳҜи—үз”ұй№Ҫзҡ„жә¶и§ЈиҖҢйҖ жҲҗи’ёж°ЈеЈ“дёӢйҷҚпјҢйҖІиҖҢйҷҚдҪҺдәҶй№Ҫж°ҙзҡ„еҮқеӣәй»һпјҢжүҖд»ҘйҖҷжҳҜжӢүеҚҲиҖіе®ҡеҫӢжүҖйҖ жҲҗзҡ„ж•ҲжҮүгҖӮдёҚйҒҺпјҢй№ҪиҲҮйӣӘйғҪжҳҜеӣәй«”пјҢжІ’жңүж¶Іж…Ӣж°ҙдҪ•дҫҶгҖҢй№Ҫзҡ„жә¶и§ЈгҖҚе‘ўпјҹйҖҷеҫһеӢ•ж…Ӣе№іиЎЎзҡ„и§Җй»һеҚіеҸҜи§ЈйҮӢгҖӮеӣ зӮәеңЁ0в„ғзҡ„еҶ°гҖҒж°ҙдәҢзӣёе…ұеӯҳжҷӮпјҢеҶ°зҡ„иіӘйҮҸиғҪдҝқжҢҒдёҚи®ҠжҳҜеӣ зӮәеҶ°зҶ”еҢ–зҡ„еҗҢжҷӮд№ҹжңғжңүж°ҙзөҗеҶ°гҖӮдҪҶжҳҜз”ұж–јжңүй№Ҫзҡ„еӯҳеңЁпјҢдёҖж—Ұж°ҙеҫһеҶ°еЎҠиЎЁйқўзҶ”еҢ–пјҢе°ұжңғз«ӢеҲ»иҲҮй№Ҫж··еҗҲпјҢз”ұж–јй№Ҫж°ҙзҡ„еҮқеӣәй»һдҪҺж–ј0в„ғпјҢеӣ жӯӨе®ғе°ұдёҚжңғзөҗеҮҚпјҢд№ҹе°ұжҳҜиӘӘеҸҜйҖҶеҸҚжҮүзҡ„平衡已經被еҠ е…Ҙзҡ„йЈҹй№ҪжүҖз ҙеЈһдәҶгҖӮ
еңЁ Instagram жҹҘзңӢйҖҷеүҮиІјж–Ү