и«ҫиІқзҲҫеҢ–еӯёзҚҺз”ұеҫ·зҫҺ2еӯёиҖ…зҚІеҫ— з ”з©¶жңүеҠ©еҢ–еӯёз”ўжҘӯжӣҙз’°дҝқ – дёӯеӨ®йҖҡиЁҠзӨҫзҷјеёғж–ј2021е№ҙ10жңҲ6ж—Ҙ
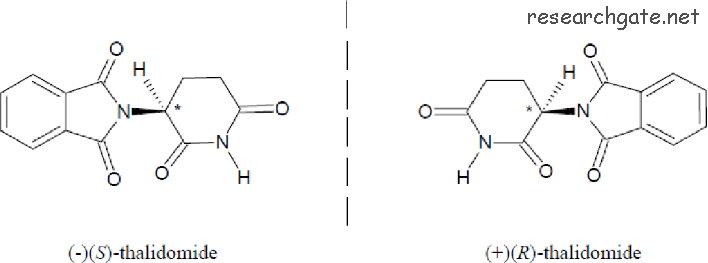
жІҷеҲ©з«ҮйӮҒпјҲThalidomideпјүжӣҫ經дҪңзӮәжҠ—еӯ•еҗҗи—Ҙзү©иў«е»ЈжіӣдҪҝз”ЁпјҢдҪҶдҪҝз”ЁеҫҢдёҚд№…пјҢзөұиЁҲж•ёж“ҡйЎҜзӨәдҪҝз”Ёи©Іи—Ҙзү©зҡ„еӯ•е©Ұд№ӢжөҒз”ўзҺҮиҲҮз•ёиғҺзҺҮдёҠеҚҮгҖӮеҫҢдҫҶз ”з©¶зҷјзҸҫи©Іи—Ҙзү©жңүе…©зЁ®е…үеӯёз•°ж§Ӣй«”пјҢе…¶дёӯзҡ„Rж§ӢеһӢжҳҜе®үе…Ёзҡ„пјҢиҖҢSж§ӢеһӢжңүиҮҙз•ёеһӢдҪңз”Ё
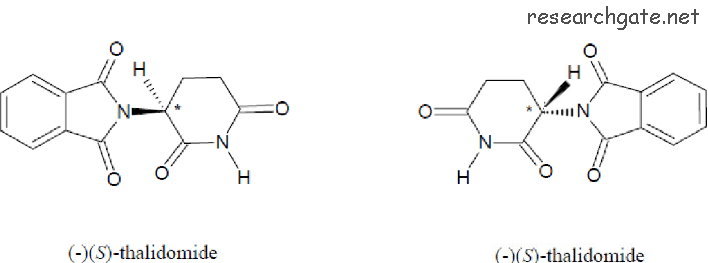
йҖҷе…©зЁ®е…үеӯёз•°ж§Ӣй«”еҸҲзЁұзӮәйҸЎеғҸз•°ж§Ӣзү©пјҢеҪјжӯӨдә’зӮәйҸЎеғҸгҖӮд»ҘдёҠең–е·Ұж–№зҡ„Sж§ӢеһӢиҖҢиЁҖпјҢйӣ–然е°Үе®ғе·ҰеҸізҝ»иҪү180еәҰеҫҢпјҢзңӢиө·дҫҶдјјд№Һе°ұи®ҠжҲҗеҸіж–№зҡ„Rж§ӢеһӢпјҢдёҚйҒҺдәҢиҖ…йӮ„жҳҜжңүжүҖе·®з•°гҖӮеӣ зӮәијғзІ—зҡ„й»‘з·ҡз«Ҝд»ЈиЎЁйӣўи§ҖеҜҹиҖ…ијғиҝ‘пјҢиҷӣз·ҡеүҮд»ЈиЎЁйҒ йӣўи§ҖеҜҹиҖ…гҖӮдёҖж—Ұе°Үе·Ұж–№зҡ„Sж§ӢеһӢе·ҰеҸізҝ»иҪү180еәҰеҫҢпјҢијғзІ—зҡ„й»‘з·ҡе°ұжңғи®ҠжҲҗиҷӣз·ҡпјҲйҖІе…ҘзҙҷйқўпјүпјҢйҖҷд»Қ然жҳҜSж§ӢеһӢиҖҢйқһRж§ӢеһӢ
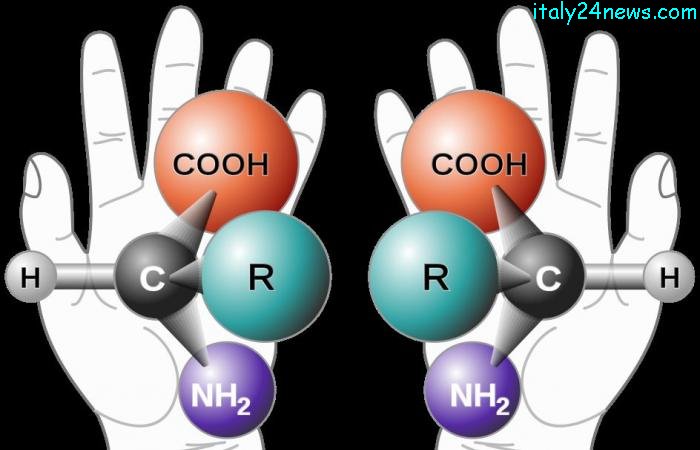
йҖҷдәҢеҖӢйҸЎеғҸз•°ж§Ӣзү©пјҢе°ұеғҸдёҖеҖӢдәәзҡ„е·ҰеҸіжүӢпјҢзӣёдјјеҚ»еҸҲдёҚеҗҢгҖӮеҰӮжһңжҠҠе…¶дёӯдёҖеҖӢеҲҶеӯҗзңӢжҲҗеҜҰзү©пјҢеүҮеҸҰдёҖеҖӢеҲҶеӯҗжҒ°еҘҪжҳҜе®ғзҡ„йҸЎеғҸпјҢйҖҷзЁ®дёҚз®ЎжҖҺжЁЈж—ӢиҪүйғҪдёҚжңғиҲҮе…¶йҸЎеғҸйҮҚеҗҲзҡ„еҲҶеӯҗпјҢе°ұеҸ«еҒҡжүӢжҖ§еҲҶеӯҗ
еңЁеҜҰй©—е®ӨдёӯйҒӢз”Ёе°Ӣеёёзҡ„ж–№жі•еҗҲжҲҗеҢ–еҗҲзү©жҷӮпјҢеӣ зӮәеӨҡеҚҠеҗҲжҲҗзҡ„ж–№жі•йғҪжҳҜе…·жңүйҸЎйқўе°ҚзЁұжҖ§пјҢеӣ иҖҢжңғеҫ—еҲ°зӯүйҮҸзҡ„е…©зЁ®йҸЎеғҸз•°ж§Ӣзү©гҖӮз”ұж–јиЈҪи—ҘйҒҺзЁӢдёӯеҗҢжҷӮж··еҗҲдәҶйҖҷе…©зЁ®ж§ӢеһӢпјҢ60е№ҙд»ЈжІҷеҲ©з«ҮйӮҒдёҠеёӮеҫҢпјҢеңЁжӯҗжҙІең°еҚҖе°ҺиҮҙеӨҡиө·йқһеёёеҡҙйҮҚзҡ„еӣӣиӮўз•ёеҪўжЎҲдҫӢпјҢзөҰиЁұеӨҡ家еәӯеё¶дҫҶе·ЁеӨ§зҡ„з—ӣиӢҰпјҢж–јжҳҜи©Іи—Ҙзү©йҡЁеҚіиў«еј·еҲ¶еҒңе”®гҖӮ
еӣ жӯӨеҝ…й ҲйҖҸйҒҺвҖңжүӢжҖ§еӮ¬еҢ–еҠ‘вҖқдҫҶиЈҪеӮҷжҹҗдёҖзЁ®ж§ӢеһӢжҜ”ијғеӨҡзҡ„йҸЎеғҸз•°ж§Ӣзү©пјҢйҖҷе°ұжҳҜжүҖи¬Ӯзҡ„вҖңдёҚе°ҚзЁұеҗҲжҲҗвҖқгҖӮ2001е№ҙпјҢи«ҫиІқзҲҫеҢ–еӯёзҚҺжҺҲдәҲдәҶдёүдҪҚеҫһдәӢжүӢжҖ§еӮ¬еҢ–з ”з©¶зҡ„科еӯёе®¶ William S. KnowlesгҖҒRyoji Noyori е’Ң K. Barry SharplessпјҢд»ҘиЎЁеҪ°д»–еҖ‘еңЁдёҚе°ҚзЁұеӮ¬еҢ–ж–№йқўеҒҡеҮәзҡ„й–ӢжӢ“жҖ§иІўзҚ»пјҢеҗҢжҷӮд№ҹеҪ°йЎҜдәҶйҖҷеҖӢй ҳеҹҹзҡ„йҮҚиҰҒжҖ§д»ҘеҸҠе°Қзӣёй—ңй ҳеҹҹеҰӮи—Ҙзү©гҖҒж–°жқҗж–ҷзӯүз”ўз”ҹзҡ„ж·ұйҒ еҪұйҹҝгҖӮз”ұж–јдҪҝз”Ёзҡ„еӮ¬еҢ–еҠ‘еҲҶеӯҗжң¬иә«жҳҜжүӢжҖ§зҡ„пјҢеӣ жӯӨеҒҸеҗ‘з”ўеҮәе…©зЁ®йҸЎеғҸеҪўејҸдёӯзҡ„дёҖзЁ®пјҢдёҰеҸҜеңЁдёҚж¶ҲиҖ—зҡ„жғ…жіҒдёӢдҫҶеҠ йҖҹеҸҚжҮүпјҢеғ…йҖҷдәӣеҲҶеӯҗдёӯзҡ„дёҖеҖӢе°ұеҸҜд»Ҙз”ўз”ҹж•ёзҷҫиҗ¬еҖӢе…·жңүжүҖйңҖйҸЎеғҸеҪўејҸзҡ„еҲҶеӯҗгҖӮд»Ҙ William S. Knowles зҡ„зҷјзҸҫзӮәдҫӢпјҢеҲ©з”Ёд»ҘDiPAMP зӮәй…ҚдҪҚеҹәзҡ„йҠ йҮ‘еұ¬(Rh)йҢҜеҗҲзү©пјҢеӮ¬еҢ–иЈҪеӮҷеҮәжІ»зҷӮеё•йҮ‘жЈ®ж°Ҹз—Үзҡ„и—Ҙзү©”L-еӨҡе·ҙ”гҖӮйҖҷзЁ®еҗ«жңүйҮ‘еұ¬йҠ зҡ„жүӢжҖ§дәҢиҶҰеӮ¬еҢ–еҠ‘еңЁж°«еҢ–еҸҚжҮүжҷӮпјҢеҸҜеҫ—еҲ°з”ўзҺҮй«ҳйҒ” 97.5% зҡ„ L-еӨҡе·ҙгҖӮжӯӨеҗҲжҲҗж–№жі•еҸҲзЁұзӮәMonsanto ProcessпјҢжҳҜ第дёҖеҖӢе•ҶжҘӯеҢ–зҡ„и—Ҙзү©иЈҪзЁӢгҖӮ
йҡЁеҫҢ Ryoji Noyori з ”з©¶еңҳйҡҠеңЁжӯӨеҹәзӨҺдёҠпјҢз ”зҷјеҮәж•ҲжһңжӣҙеҘҪзҡ„дёҚе°ҚзЁұж°«еҢ–еҸҚжҮүж–№жі•еҸҠжҖ§иғҪжӣҙзӮәе„Әз•°зҡ„еӮ¬еҢ–еҠ‘пјҢд»Ҙ BINAP зӮәй…ҚдҪҚеҹәзҡ„йҠ йҮ‘еұ¬йҢҜеҗҲзү©йҖІиЎҢдёҚе°ҚзЁұжҖ§ж°«еҢ–еӮ¬еҢ–еҸҚжҮүпјҢеҗҲжҲҗеҮәдёҖдәӣе…үеӯёзҙ”еәҰ ee еҖјй«ҳйҒ” 100% зҡ„иғәеҹәй…ёгҖӮйҮҺдҫқиүҜжІ»зҡ„з ”з©¶жҲҗжһңпјҢзҸҫд»Ҡиў«е»Јжіӣең°йҒӢз”ЁеңЁеҫҲеӨҡеҢ–еӯёиЈҪе“ҒгҖҒи—Ҙзү©е’Ңж–°жқҗж–ҷзҡ„иЈҪйҖ гҖӮ
еңЁиҘҝе…ғ2000 е№ҙд»ҘеүҚпјҢжңҖеёёз”Ёзҡ„жүӢжҖ§еӮ¬еҢ–еҠ‘еҗ«жңүйҮҚйҮ‘еұ¬йҠ е’ҢйҮ•пјҢдёҚеғ…йқһеёёжҳӮиІҙпјҢд№ҹеҸҜиғҪжңүжҜ’пјҢеҗҢжҷӮйңҖиҰҒйқһеёёзү№ж®Ҡзҡ„еҜҰй©—жўқ件гҖӮ2000 е№ҙпјҢзҫҺеңӢжҷ®жһ—ж–Ҝй “еӨ§еӯё David MacMillan ж•ҷжҺҲиЁӯиЁҲдәҶеҸҜд»ҘжҸҗдҫӣжҲ–жҺҘеҸ—йӣ»еӯҗеҫһиҖҢжңүж•ҲеӮ¬еҢ–еҸҚжҮүзҡ„жңүж©ҹе°ҸеҲҶеӯҗпјҢй–ӢзҷјеҮәеҸҜд»Ҙй©…еӢ•дёҚе°ҚзЁұеӮ¬еҢ–пјҲAsymmetric catalysisпјүзҡ„жңүж©ҹеӮ¬еҢ–еҠ‘пјҢдәҰеҚідёҚеҗ«жңүйҮ‘еұ¬гҖӮжңүж©ҹеӮ¬еҢ–еҠ‘е…·жңүдёҖеҖӢз©©е®ҡзҡ„зўіеҺҹеӯҗжЎҶжһ¶пјҢеҸҜд»Ҙи®“жӣҙжҙ»иәҚзҡ„еҢ–еӯёеҹәеңҳйҷ„и‘—еңЁдёҠйқўгҖӮе®ғеҖ‘йҖҡеёёеҗ«жңүдёҖдәӣеёёиҰӢе…ғзҙ пјҢеҰӮж°§гҖҒж°®гҖҒзЎ«жҲ–зЈ·пјҢйҖҷж„Ҹе‘іи‘—йҖҷдәӣеӮ¬еҢ–еҠ‘ж—ўз’°дҝқеҸҲдҫҝе®ңгҖӮDavid MacMillan йҒёж“ҮдәҶе№ҫеҖӢе…·жңүеҗҲйҒ©жҖ§иіӘзҡ„жңүж©ҹеҲҶеӯҗпјҢжё¬и©ҰдәҶе®ғеҖ‘й©…еӢ•В зӢ„иҖіеЈ«вҖ“йҳҝзҲҫеҫ·еҸҚжҮүпјҲDielsвҖ“Alder reactionпјү зҡ„иғҪеҠӣпјҢеҢ–еӯёе®¶еҖ‘з”ЁйҖҷзЁ®еҸҚжҮүдҫҶиЈҪйҖ зўіеҺҹеӯҗз’°гҖӮзөҗжһңжӯЈеҰӮд»–жүҖй җжё¬зҡ„йӮЈжЁЈпјҢйҖҷдёҖж–№жі•йқһеёёжңүж•ҲпјҢжҹҗдәӣжңүж©ҹеҲҶеӯҗеңЁдёҚе°ҚзЁұеӮ¬еҢ–ж–№йқўеҫҲеҮәиүІпјҢеңЁе…©зЁ®еҸҜиғҪзҡ„йҸЎеғҸз”ўзү©дёӯпјҢе…¶дёӯдёҖзЁ®дҪ”ж“ҡдәҶз”ўзү©зҡ„ 90% д»ҘдёҠгҖӮжҜ”еҰӮ DMI йҖҷзЁ®жүӢжҖ§зҡ„е’Әе”‘е•үй…®еӮ¬еҢ–еҠ‘пјҲ1,3-Dimethyl-2-imidazolidinoneпјүвҶ’В жүӢжҖ§е’Әе”‘е•үй…®йЎһжңүж©ҹеӮ¬еҢ–еҠ‘еӮ¬еҢ–зҡ„дёҚе°ҚзЁұеҸҚжҮүгҖӮMacMillan зҡ„з ”з©¶е°Ҹзө„йҡЁеҫҢеңЁдёҚе°ҚзЁұжңүж©ҹеӮ¬еҢ–пјҲOrganocatalysisпјүй ҳеҹҹеҸ–еҫ—дәҶиЁұеӨҡйҖІеұ•пјҢдёҰе°ҮйҖҷдәӣж–°ж–№жі•жҮүз”Ёж–јдёҖзі»еҲ—иӨҮйӣңеӨ©з„¶з”ўзү©зҡ„еҗҲжҲҗпјҢзӮәжңүж©ҹеӮ¬еҢ–й ҳеҹҹеҒҡеҮәдәҶиІўзҚ»гҖӮ
дёӢеүҮеҪұзүҮеүҮд»Ҙжңүж©ҹй…ёеӮ¬еҢ–зҡ„ж°ҙзҶұеҸҚжҮүдҫҶеҲҶйӣўж··зҙЎдёҚеҗҢжқҗиіӘзҡ„зә–з¶ӯпјҢйҖҷжҳҜдҪҝз”Ёеҗ«жңүзЎ«й…ёгҖҒзЈ·й…ёиҲҮеҶ°йҶӢй…ёзҡ„ж··еҗҲзү©з•¶еӮ¬еҢ–еҠ‘пјҢйҖІиЎҢи„«д№ҷйҶҜдҪңз”Ёи®“зә–з¶ӯзҙ дё»йҸҲж°ҙи§Ј
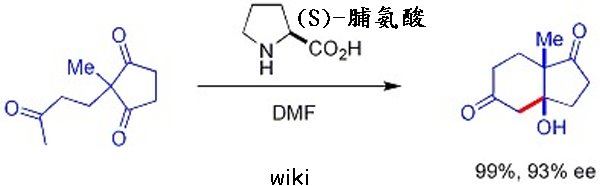
еҫ·еңӢйҰ¬е…Ӣж–Ҝжҷ®жң—е…Ӣз ”з©¶жүҖжүҖй•· Benjamin List еүҮжҳҜеҫһиғәеҹәй…ёдҫҶзҷјжғігҖӮд»–жҸҗеҮәдёҖеҖӢеҒҮиЁӯпјҡиғәеҹәй…ёеҝ…й ҲжҳҜй…¶зҡ„дёҖйғЁеҲҶжүҚиғҪеӮ¬еҢ–еҢ–еӯёеҸҚжҮүе—ҺпјҹдёҖеҖӢе–®зҚЁзҡ„иғәеҹәй…ёпјҢжҲ–иҖ…жҳҜйЎһдјјзҡ„з°Ўе–®еҲҶеӯҗпјҢд№ҹиғҪиө·еҲ°еҗҢжЁЈзҡ„дҪңз”Ёе—ҺпјҹBenjamin List зҹҘйҒ“ж—©еңЁ 20 дё–зҙҖ 70 е№ҙд»ЈпјҢе°ұжңүдёҖй …з ”з©¶е°Үи„Ҝ氨酸當дҪңеӮ¬еҢ–еҠ‘зҡ„еҲҶеӯҗе…§зҫҘйҶӣеҸҚжҮүпјҢз”ўзү©жҳҜйӣҷз’°й…®йҶҮ
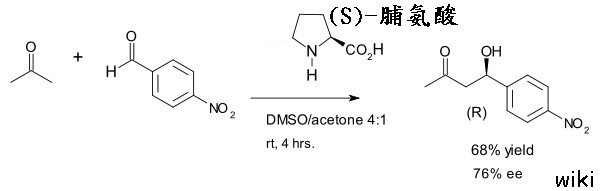
еҰӮжһңи„Ҝж°Ёй…ёзңҹзҡ„жҳҜдёҖзЁ®жңүж•Ҳзҡ„еӮ¬еҢ–еҠ‘пјҢйӮ„жңғжңүдәәз№јзәҢз ”з©¶е®ғе—ҺпјҹеңЁжҹҗзЁ®зЁӢеәҰдёҠпјҢBenjamin List д№ҹжҳҜйҖҷйәјжғізҡ„гҖӮд»–иӘҚзӮәпјҢжІ’жңүдәәз№јзәҢз ”з©¶йҖҷеҖӢзҸҫиұЎзҡ„еҺҹеӣ пјҢжҳҜйҖҷзЁ®иғәеҹәй…ёеңЁдёҚеҗҢе…©еҖӢеҲҶеӯҗй–“зҡ„еӮ¬еҢ–ж•ҲжһңйҖҡеёёдёҚеӨӘеҘҪгҖӮеңЁдёҚжҠұд»»дҪ•жңҹжңӣзҡ„жғ…жіҒдёӢпјҢж–јжҳҜд»–жё¬и©ҰдәҶи„Ҝж°Ёй…ёжҳҜеҗҰиғҪеӮ¬еҢ–еҲҶеӯҗй–“зҡ„ зҫҘйҶӣеҸҚжҮүпјҢд»Өдәәй©ҡиЁқзҡ„жҳҜи„Ҝж°Ёй…ёз«ӢеҚізҷјжҸ®дәҶдҪңз”ЁгҖӮйҒёз”Ёзҡ„(S)-и„Ҝж°Ёй…ёдҫҶеҒҡдёҷй…®е’Ңе°ҚзЎқеҹәиӢҜз”ІйҶӣзҡ„еҲҶеӯҗй–“зӣҙжҺҘзҫҘйҶӣеҸҚжҮүжҷӮпјҢеҜҰзҸҫдәҶ68пј…з”ўзҺҮгҖҒ76пј…eeеҖјгҖӮйҖҷжЁҷиӘҢи‘—жңүж©ҹеӮ¬еҢ–еҫ©иҲҲзҡ„й–Ӣе§ӢпјҢйҖҷзЁ®жңүж©ҹеӮ¬еҢ–зҡ„еҲҶеӯҗй–“зҫҘйҶӣеҸҚжҮүд№ҹиў«зЁұзӮә List-Barbas зҫҘйҶӣеҸҚжҮү
Benjamin List дёҚеғ…йҖҡйҒҺеҜҰй©—иӯүжҳҺдәҶи„Ҝж°Ёй…ёжҳҜдёҖзЁ®й«ҳж•Ҳзҡ„еӮ¬еҢ–еҠ‘пјҢйӮ„иӯүжҳҺдәҶйҖҷзЁ®иғәеҹәй…ёеҸҜд»Ҙй©…еӢ•дёҚе°ҚзЁұеӮ¬еҢ–гҖӮ當 Benjamin List еңЁ 2000 е№ҙ 2 жңҲзҷјиЎЁйҖҷдәӣзҷјзҸҫжҷӮпјҢд»–е°Үжңүж©ҹеҲҶеӯҗзҡ„дёҚе°ҚзЁұеӮ¬еҢ–жҸҸиҝ°зӮәдёҖеҖӢиғҪеё¶дҫҶеӨ§йҮҸж©ҹжңғзҡ„ж–°жҰӮеҝөпјҡвҖңTheВ design and screening of these catalysts is one of our future aimsвҖқгҖӮжӯӨеҫҢдёҖеҖӢж–°зҡ„еҢ–еӯёеҲҶж”ҜиӘ•з”ҹдәҶпјҢдёҚе°ҚзЁұжңүж©ҹеӮ¬еҢ–пјҲAsymmetric OrganocatalysisпјүгҖӮеңЁжңүж©ҹеҸҚжҮүдёӯпјҢзӮәдәҶеҠ йҖҹеҸҚжҮүзҡ„йҖІиЎҢ經常й Ҳж·»еҠ дёҖдәӣеӮ¬еҢ–еҠ‘пјҢ然иҖҢйҖҷдәӣеӮ¬еҢ–еҠ‘еёёеёёжҳҜеҗ«жңүйҮҚйҮ‘еұ¬зҡ„жҲҗеҲҶпјҢиӢҘиҷ•зҗҶдёҚ當жңғе°ҺиҮҙз’°еўғзҡ„жұЎжҹ“гҖӮжӣҙдёҚз”ЁиӘӘеңЁжҹҗдәӣе·ҘжҘӯеҢ–еӯёеҸҚжҮүдёӯпјҢи¶…йҒҺ50% зҡ„жҲҗжң¬жҳҜиҲҮйҮ‘еұ¬еӮ¬еҢ–еҠ‘зҡ„дҪҝз”Ёе’Ңиҷ•зҪ®жңүй—ңгҖӮеӣ жӯӨпјҢдёҚдҪҝз”ЁйҒҺжёЎйҮ‘еұ¬пјҢдёҖеҲҮйғҪи®Ҡеҫ—жӣҙз’°дҝқиҲҮ經жҝҹпјҢжҲ‘еҖ‘зөӮж–јиҪүеҗ‘дәҶз¶ иүІе’Ңз”ҹж…ӢеҸҜжҢҒзәҢзҡ„еҢ–еӯёпјҒ
延伸й–ұи®Җ
зӮәд»ҖйәјдёҚе°ҚзЁұжңүж©ҹеӮ¬еҢ–иғҪзҚІеҫ—и«ҫиІқзҲҫеҢ–еӯёзҚҺпјҹ